Содержание
- 1 Статьи по теме:
- 2 Когда необходимо хирургическое вмешательство?
- 3 Страх перед операцией
- 4 Трансназальная аденомэктомия — через нос
- 5 Краниотомия — трепанация черепа
- 6 Радиохирургия
- 7 Возможные осложнения
- 8 Восстановление после операции
- 9 Эпидемиология: причины, частота заболеваемости
- 10 Классификация аденом гипофиза головного мозга
- 11 Клинические проявления опухоли
- 12 Методы диагностики патологии
- 13 Принципы лечения заболевания
- 14 Трансназальная операция по удалению аденомы гипофиза головного мозга
- 15 Заключение
Наиболее демонстративно последствия выпадения функции передней доли гипофиза проявляются после оперативного удаления гипофиза, производимого с лечебной целью при некоторых заболеваниях. В настоящее время накоплено значительное количество наблюдений над такими больными.
Несмотря на то, что такая патология встречается все же редко, могут быть проанализированы основные проявления синдрома, связанного с выпадением функции передней доли гипофиза без повреждения центров гипоталамуса, и основные принципы лечения этих больных.
Наиболее существенным нарушением, представляющим опасность для жизни больного после удаления гипофиза, является понижение функции коры надпочечников. Недостаточность надпочечников может возникнуть уже через 36 ч после операции, но иногда развивается постепенно на протяжении 3-4 недель. Вторичный гипокортицизм после удаления гипофиза имеет некоторые особенности по сравнению с гипокортицизмом в связи с первичным поражением надпочечников. Выпадает преимущественно гликокортикоидная функция надпочечников, в то время как продукция альдостерона страдает относительно мало. Это явление вполне объяснимо в свете имеющихся данных об относительной независимости клубочковой зоны надпочечников, в которой вырабатывается альдостерон, от гипофизарной регуляции.
У больных после удаления гипофиза появляется анорексия, тошнота и рвота, резкая слабость, адинамия, сонливость; может иметь место гипертермия. Артериальное давление снижается, появляется ортостатическая гипотония, и может развиться сосудистый коллапс. Солевой обмен существенно не нарушается. Больные, получающие заместительную терапию кортизоном, нормально реагируют на ограничение в пище натрия уменьшением выделения натрия мочой.
Развитие гипотонии у больных после гипофизэктомии при преимущественном выпадении секреции гликокортикоидов и при относительно сохраненной продукции альдостерона, по-видимому, объясняется тем, что выпадает пермессивное действие гликокортикоидов, необходимое для проявления гипертензивных влияний.
Пигментация у больных с недостаточностью коры надпочечников вследствие удаления гипофиза отсутствует в связи с тем, что выделение у них не повышено. Однако у этих больных отсутствует и характерная бледность, свойственная больным с пангипопитуитаризмом.
У больных после удаления гипофиза закономерно снижается функция половых желез. У женщин прекращаются менструации, и через несколько недель развиваются глубокие атрофические изменения половых органов и молочных желез. У мужчин через 4-6 недель после операции наблюдается атрофия яичек и наружных половых органов, наступает импотенция. Половое чувство исчезает у лиц обоего пола. Прекращают расти и выпадают волосы в подмышечных областях и на лобке. Волосы на голове делаются более тонкими.
Понижение функции щитовидной железы наступает менее закономерно и более постепенно, чем понижение функции коры надпочечников и половых желез. У большинства больных гипотиреоз развивается через 1-6 месяцев после удаления гипофиза. Первыми признаками развивающегося гипотиреоза являются сухость кожи и прибавка веса. Позднее появляются зябкость, запоры, вялость, заторможенность, утолщение кожи. Существенного повышения уровня холестерина у больных со вторичным гипотиреозом вследствие удаления гипофиза в отличие от больных с первичным гипотиреозом в связи с поражением щитовидной железы обычно не наблюдается.
Наряду с этим, у некоторых больных после удаления гипофиза отсутствовали клинические и лабораторные признаки гипотиреоза на протяжении 6-24 месяцев наблюдения после операции. У некоторых из этих больных имелись гиперфункционирующие аденомы щитовидной железы, в отдельных случаях щитовидная железа была нормальной. В случае неполного удаления гипофиза наблюдается лишь преходящее понижение функции щитовидной железы.
Если удаление гипофиза произведено в пределах турецкого седла ниже его диафрагмы и гипоталамус остается неповрежденным, стойкий несахарный диабет не развивается. Такие больные вследствие понижения секреции гликокортикоидов корой надпочечников обладают пониженной толерантностью к водной нагрузке, подобно больным аддисоновой болезнью. Если же несахарный диабет развился в связи с повреждением проксимальных отделов нейрогипофиза или ядер гипоталамуса, диурез относительно невелик при отсутствии заместительной терапии кортизоном и значительно повышается после введения кортизона.

Статьи по теме:
Углеводный обмен после удаления гипофиза изменяется мало. Отмечается лишь небольшое снижение сахара крови натощак, углубление гипогликемической фазы после углеводной нагрузки; чувствительность к инсулину немного повышается. У больных сахарным диабетом после удаления гипофиза существенно снижается потребность в инсулине. Это связано не с выпадением адренокортикотропной функции гипофиза, так как повышенная чувствительность к инсулину сохраняется у больных, получающих лечение кортизоном, а с прекращением секреции аденогипофизом гормона роста.
Введение больным сахарным диабетом с удаленным гипофизом гормона роста оказывает выраженное диабетогенное действие.
Способность к заживлению ран и переломов у больных послеудаления гипофиза сохраняется. Изменения в обмене кальция и фосфора отсутствуют. Вес тела существенно не меняется, хотя имеется некоторая тенденция к прибавлению веса.
Удаление аденомы гипофиза – это чаще всего необходимость, поскольку новообразование провоцирует развитие серьезных осложнений, а иногда и рак. В большинстве случаев вмешательство производят через нос либо через разрез в ротовой полости. В тяжелых ситуациях назначают вскрытие черепной коробки для удаления опухоли.

Когда необходимо хирургическое вмешательство?
Уплотнение внутреннего органа обычно оказывает отрицательное воздействие на гормональный фон. Оно увеличивает или уменьшает выработку некоторых гормонов, что приводит к появлению неприятных симптомов. Чтобы предотвратить развитие серьезных осложнений и переход в злокачественное новообразование, врачи назначают операцию по удалению.
Однако хирургическое вмешательство проводят не всегда. Для этого аденома должна проявлять гормональную активность. Иногда назначают поддерживающую консервативную терапию. Но иногда без оперативного воздействия не обойтись. Показаниями к нему считаются следующие факторы:

- капсула относится к гормонально-активному типу и отрицательно сказывается на гормональном фоне. Она вызывает нарушение правильного продуцирования биологически активных веществ;
- крупного размера утолщения сдавливают соседние ткани, провоцируя ухудшение зрения;
- опухоль крупная и продолжает расти. Медикаментозное лечение не дало результатов.
Окончательное решение о целесообразности хирургического вмешательства принимает лечащий врач. Для этого он изучает результаты МРТ и прочих видов обследования.
Страх перед операцией
Оперативное воздействие, особенно в области железы, сопряжено с определенным риском. Чтобы избежать осложнений, нужно довериться профессиональному хирургу, специализирующемуся на подобных типах новообразований. При условии своевременного удаления патологических тканей риск неприятных последствий сводится к минимуму.
Трансназальная аденомэктомия — через нос
Удаление производится несколькими способами. Наиболее распространенный метод предусматривает введение через носовой проход эндоскопа. Оборудование содержит миниатюрную видеокамеру, при помощи которой врач полностью контролирует все манипуляции.
Этот тип воздействия используется при капсулах небольшого размера и считается малотравматичным. Трансназальное удаление аденомы гипофиза проводится и через левую, и через правую ноздрю. Хирург вводит в полость оборудование, диаметр которого составляет не больше 0,5 см. Картинка выводится на экран.

Чтобы провести процедуру, перерезают стенки в пазухе, в турецком седле делают отверстие, через которое в дальнейшем удаляют утолщение. Если опухоль чуть больше среднего размера, ее удаляют частями.
После процедуры останавливают кровотечение. Стерильные тампоны обрабатывают дезинфицирующими растворами, вводят их внутрь. Также используется электрокоагуляция, при которой ткани быстро прижигают. В дальнейшем турецкое седло восстанавливают, используя для этого натуральные материалы или искусственные. После операции пациент сможет покинуть больницу уже через несколько дней.
Краниотомия — трепанация черепа
Этот способ не самый популярный в силу высокого риска развития осложнений. Его используют, если аденома значительно увеличилась в размерах или находится за границей турецкого седла. Это делает удаление через носовые пазухи невозможным. Краниотомия – это манипуляция, при которой доступ к опухоли осуществляют через черепные кости.
Во время вмешательства проводится трепанация черепа. Доступ к гипофизу получают либо через височные доли, либо через лобную часть. Это зависит от места локализации полости и иных особенностей. В ходе манипуляции вводят общее обезболивание.
Пациента помещают на бок, вскрывают черепную коробку и иссекают твердую оболочку мозга. Когда хирург добирается до железы, он использует ультразвуковой аспиратор либо электрический пинцет. С их помощью удаляют содержимое капсулы. В редких случаях приходится вырезать не только аденому, но и сам гипофиз. Обычно это происходит, если разросшаяся ткань проникла глубоко во внутренний орган.
После проведения операции прижигают сосуды, чтобы остановить кровотечение. Затем врач возвращает на место фрагмент кости черепа, накладывает скрепляющие швы. Вся процедура занимает около 4 часов. В течение суток за пациентом наблюдают в отделении реанимации, чтобы исключить развитие осложнений. Еще 1 – 1,5 недели он проведет в стационаре, где будет восстанавливаться.
Краниотомия дает результат почти в 70% случаев. Но, чем больше размер новообразования, тем выше риск развития послеоперационных осложнений. После вмешательства иногда происходит рецидив болезни. Более чем в 20% случаев на гипофизе вновь образуется опухоль.
Радиохирургия
Этот метод назначают, если аденома небольшого диаметра. Малотравматичная операция позволяет избежать воздействия на здоровые ткани. Пациент не испытывает боли и очень быстро восстанавливается

Радиохирургия предусматривает использование киберножа для доступа к гипофизу. В ходе процедуры пациент находится в лежачем положении, а на череп точечно воздействуют лучами. Излучение останавливает разрастание тканей, уменьшает размер капсулы. Вмешательство занимает чуть больше получаса, затем человек покидает больницу. Неприятные ощущения при осуществлении воздействия отсутствуют.
Это самый безопасный способ удаления, однако и самый дорогой. Манипуляцию не проводят бесплатно. В частных клиниках стоимость операции достигает 100 тысяч рублей и более. Муниципальные учреждения не располагают необходимым оборудованием.
Возможные осложнения
Любая операция по удалению аденомы гипофиза сопряжена с определенным риском. Наиболее безопасным методом является радиохирургия. За ней следует трансназальная аденомэктомия. Краниотомия – самый рисковый вид процедуры, после которого пациенты чаще всего сталкиваются с неприятными последствиями. После хирургического воздействия могут возникнуть следующие осложнения:
-
хирург заденет здоровые ткани внутреннего органа или соседние клетки. Это скажется на дальнейших связях гипоталамо-гипофизарного отдела. Нарушение деятельности приводит к серьезным гормональным сбоям, невозможности наступления беременности, болезням щитовидки;


Большинство этих осложнений развиваются при проведении краниотомии. Удаление проводится без использования эндоскопического оборудования, и все зависит только от квалификации врача.
Восстановление после операции
Успешность восстановления после удаления новообразования зависит от его размеров, дополнительных особенностей. В большинстве случаев человек реабилитируется и может вести привычную жизнь. При развитии серьезных осложнений происходит частичная утрата некоторых функций. В наиболее тяжелых ситуациях не исключается летальный исход.
Восстановительный период при аденоме гипофиза после операции длится в среднем несколько недель. Продолжительность зависит от типа проведенного вмешательства. В течение всего срока нужно соблюдать несколько общих рекомендаций:

- избегать переутомления, физической активности или нагрузки;
- соблюдать все врачебные предписания;
- не применять гормональные препараты или прочие медикаменты, если их не назначил лечащий врач;
- не использовать народные средства восстановления без предварительной консультации;
- проходить плановые осмотры;
- женщинам в период лактации свернуть грудное вскармливание.
Оперативное удаление опухоли на внутреннем органе – процедура, сопряженная с долей риска. Но нельзя игнорировать патологию и не лечиться. Отсутствие терапии спровоцирует ухудшение самочувствия и может привести к более серьезным последствиям, чем хирургическое вмешательство.

Автор: Насруллаев Мурад
Кандидат медицинских наук, врач маммолог-онколог, хирург
Аденома гипофиза головного мозга (АГГМ) представляет собой опухоль железистой ткани мозгового придатка. Гипофиз – это значимая в организме человека эндокринная железа, располагающаяся в нижней части мозга в гипофизарной ямке турецкого седла. Этот маленький орган эндокринной системы, у взрослого человека весом всего в 0,7 г, отвечает за собственную продукцию гормонов и контроль над синтезом гормонов щитовидной и паращитовидной железой, мочеполовыми органами. Гипофиз участвует в регуляции водно-жирового обмена, отвечает за рост и вес человека, развитие и работу внутренних органов, начало родовой деятельности и лактацию, становление репродуктивной системы и др. Не зря эту железу медики величают «виртуозным дирижером», управляющим звучанием большого оркестра, где оркестр – это весь наш организм.
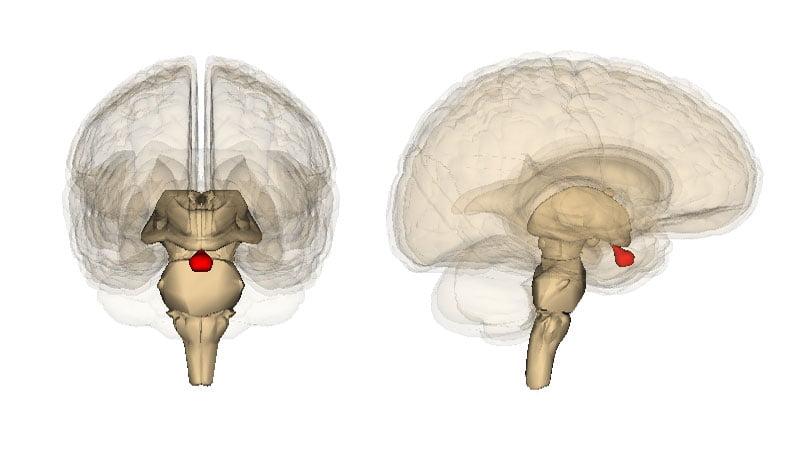
Схематичное изобрадение расположения опухоли.
Но, к сожалению, уникальный орган, без которого слаженный функциональный баланс в организме невозможен, не защищен от патологических образований, или болезней на почве гормонального и/или неврогенного расстройства. Одним из серьезных заболеваний является аденома, при которой железистый, гормонально активный эпителий гипофиза головного мозга патологически разрастается, что может стать причиной инвалидизации больного.
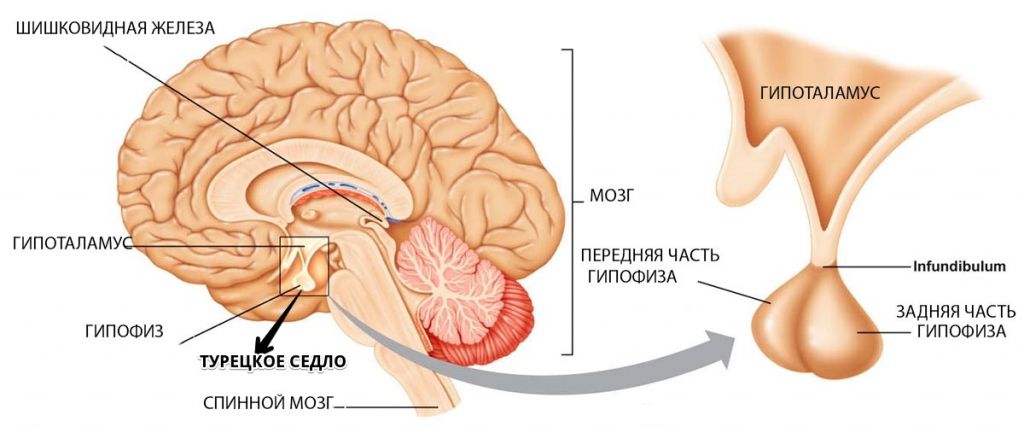
Аденомы могут быть активными (ААГ) и неактивными (НАГ). В первом случае страдает гормональный фон от переизбытка выделяемых гипофизарных гормонов. Во втором – массив опухоли раздражает, сдавливает близко расположенные ткани, чаще затрагивается зрительный нерв. Стоит отметить, что сильно увеличенные пропорции и активного патологического очага так же негативно воздействуют на внутричерепные ткани, находящиеся вблизи. О других особенностях патологии, включая специфику лечения, предлагаем узнать из статьи.
Эпидемиология: причины, частота заболеваемости
Фактор, который стимулирует развитие гипофизарной опухоли, до сих пор не выявлен, поэтому остается главным предметом исследований. Специалисты относительно вероятных причин озвучивают лишь версии:
- черепно-мозговые травмы;
- нейроинфекция головного мозга;
- пагубные привычки;
- беременность 3 и более раз;
- наследственность;
- прием гормональных препаратов (например, контрацептивов);
- хронические стрессы;
- артериальная гипертензия и др.
Новообразование встречается не так уж и редко, в общей структуре опухолей головного мозга на его долю приходится 12,3%-20% случаев. По частоте встречаемости оно занимает 3 место среди нейроэктодермальных неоплазий, уступая лишь глиальным опухолям и менингиомам. Заболевание, как правило, доброкачественной природы. Однако в медицинской статистике зафиксированы данные о единичных случаях злокачественной трансформации аденомы с образованием вторичных очагов (метастазов) в головной мозг.
Патологический процесс чаще диагностируется у женщин (примерно в 2 раза больше), чем у мужчин. Далее приведем данные о распределении возрастов из расчета 100% пациентов с клинически подтвержденным диагнозом. Эпидемиологический пик приходится на возраст 35-40 лет (до 40%), в 30-35 лет заболевание определяется у 25% пациентов, в 40-50 лет – у 25%, 18-35 и старше 50 лет – по 5% на каждую возрастную категорию.
По статистике, около 40% пациентов имеют неактивную опухоль, которая не секретирует в избытке гормональные вещества и не отражается на эндокринном равновесии. Приблизительно у 60% пациентов определяют активное образование, отличающееся гиперсекрецией гормонов. Порядка 30% людей становятся инвалидами из-за последствий агрессивной гипофизарной аденомы.
Классификация аденом гипофиза головного мозга
Гипофизарный очаг формируется в передней доли железы (в аденогипофизе), которая составляет основную массу органа (70%). Развивается заболевание при мутации одной клетки, как результат, она выходит из-под иммунного надзора и выпадает из физиологического ритма. Впоследствии, путем многократного деления клетки-предшественника образуется аномальное разрастание, состоящее из группы идентичных (моноклональных) клеток. Это и есть аденома, такой механизм развития самый частый. Однако в редких случаях очаг может изначально происходить из одного клеточного клона, а после рецидива – из другого.
Патологические образования различают по активности, величине, гистологии, характеру распространения, виду секретируемых гормонов. Мы уже выяснили, какого вида активности бывают аденомы, – гормонально-активные и гормонально-неактивные. Рост дефектной ткани характеризует параметр агрессивности: опухоль может быть неагрессивной (небольшая и не склонная к увеличению) и агрессивной, когда она достигает больших размеров и оказывает инвазию на соседние структуры (артерии, вены, нервные ветви, пр.).
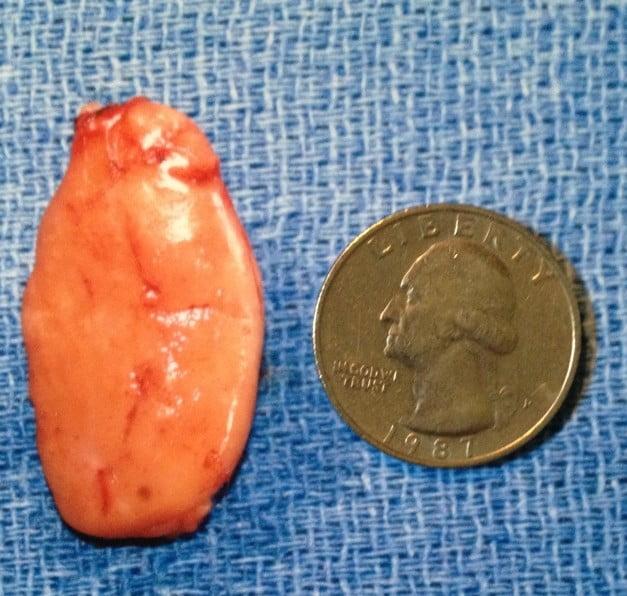
Крупная аденома после удаления.
По величине аденомы гипофиза ГМ бывают следующих видов:
- микроаденомы (менее 1 см в диаметре);
- мезоаденомы (1-3 см);
- большие (3-6 см);
- гигантские аденомы (размером более 6 см).
АГГМ по распространению делятся на:
- эндоселлярные (в пределах гипофизарной ямки);
- эндоэкстраселлярные (с выходом за ориентиры седла), которые распространяются:
► супраселлярно – в полость черепа;
► латероселлярно – в пещеристый синус или под твердую мозговую оболочку;
► инфраселлярно – растут вниз в сторону клиновидной пазухи носа/носоглотки;
► антеселлярно – затрагивают решетчатый лабиринт и/или глазницу;
► ретроселлярно – в заднюю черепную ямку и/или под Блюменбахов скат.
По гистологическому признаку аденомам присвоены наименования:
- хромофобные – неоплазии, образованные бледными, нечетко контурируемыми аденогипофизарными клетками хромофобами (распространенный тип, представлен НАГ);
- ацидофильные (эозинофильные) – опухоли, сотворенные альфа-клетками с хорошо развитым синтетическим аппаратом;
- базофильные (мукоидные) – неопластические образования, развивающиеся из базофильных (бета-клеток) аденоцитов (наиболее редкая опухоль).
Среди гормонально-активных аденом различают:
- пролактиномы – активно секретируют пролактин (самый частый вид);
- соматотропиномы – в избытке продуцируют соматотропный гормон;
- кортикотропиномы – стимулируют выработку адренокортикотропина;
- гонадотропиномы – усиливают синтез гонадотропина хорионического;
- тиреотропиномы – дают большой выброс ТТГ, или тиреотропного гормона;
- комбинированные (полигормональные) – секретируют от 2 и более гормонов.
Клинические проявления опухоли
Многие симптомы пациентами, как они сами подчеркивают, поначалу не воспринимаются серьезно. Недомогания зачастую связывают с банальным переутомлением или, к примеру, стрессом. Действительно, проявления могут быть неспецифичными и завуалированными долгое время – 2-3 года или больше. Заметим, что характер и интенсивность симптомов зависят от степени агрессии, вида, локализации, объема и многих других характеристик аденомы. Клиника новообразования складывается из 3 симптоматических групп.
- Неврологические признаки:
- головная боль (ее испытывает большая часть пациентов);
- нарушенная иннервация глазных мышц, что вызывает глазодвигательные расстройства;
- болезненные ощущения по ходу ветвей тройничного нерва;
- симптомы гипоталомического синдрома (ВСД-реакции, психическая неуравновешенность, проблемы с памятью, фиксационная амнезия, бессонница, нарушение волевой активности, пр.);
- проявления окклюзионно-гидроцефального синдрома в результате блокады оттока ликвора на уровне межжелудочкового отверстия (нарушение сознания, сна, приступы головной боли при движении головой, др.).
- Офтальмологические симптомы по невральному типу:
- ощутимое расхождение в остроте зрения одного глаза от другого;
- постепенное падение зрения;
- исчезновение верхних полей восприятия в обоих глазах;
- выпадение поля видения назальных или височных областей;
- атрофические изменения глазного дна (определяются офтальмологом).
- Эндокринные проявления в зависимости от продукции гормонов:
- гиперпролактинемия – выделение молозива из груди, аменорея, олигоменорея, бесплодие, поликистоз яичников, эндометриоз, снижение либидо, оволосение, самопроизвольные аборты, у мужчин проблемы с потенцией, гинекомастия, низкое качество спермы для зачатия и др.;
- гиперсоматотропизм – увеличение в размерах дистальных отделов конечностей, надбровных дуг, носа, нижней челюсти, скул или внутренних органов, осиплость и огрубение голоса, дистрофия мышц, трофические изменения в суставах, миалгии, гигантизм, ожирение и прочее;
- синдром Иценко-Кушинга (гиперкортицизм) – диспластическое ожирение, дерматозы, остеопороз костей, переломы позвоночника и ребер, дисфункция репродуктивных органов, гипертензия, пиелонефрит, стрии, иммунодефицитные состояния, энцефалопатия;
- симптомы гипертиреоза – повышенная раздражительность, беспокойный сон, переменчивое настроение и тревожность, похудение, дрожание кистей рук, гипергидроз, перебои сердечного ритма, высокий аппетит, кишечные расстройства.
Примерно у 50% людей на фоне гипофизарной аденомы возникает симптоматический (вторичный) диабет. У 56% диагностируют утрату зрительных функций. В той или иной мере почти все испытывают классические для гипофизной гиперплазии головного мозга симптомы: головная боль (более чем у 80%), психоэмоциональные, метаболические, сердечно-сосудистые расстройства.
Методы диагностики патологии
Специалисты придерживаются единой схемы диагностики при подозрении у человека этого диагноза, которая предусматривает:
- осмотр у невролога, эндокринолога, окулиста, ЛОР-врача;
- проведение лабораторных анализов – общее исследование крови и мочи, биохимия крови, тесты крови на сахар и концентрацию гормонов (пролактин, ИФР-1, кортикотропин, ТТГ-Т3-Т4, гидрокортизон, женские/мужские половые гормоны);
- обследование сердца на ЭКГ-аппарате, УЗИ внутренних органов;
- ультразвуковое исследование сосудов вен нижних конечностей;
- рентген костей черепа (краниография);
- компьютерную томографию мозга, в отдельных случаях возникает дополнительная потребность в МРТ.
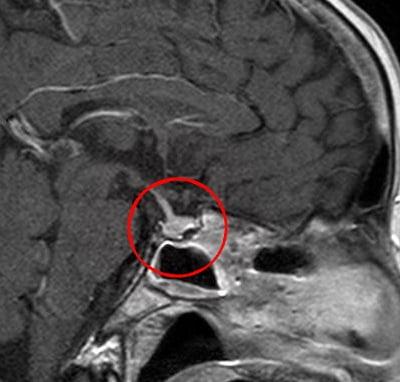
Отметим, что специфика забора и изучения биологического материала на гормоны состоит в том, что выводов не делают после первого же обследования. Для достоверности гормональной картины необходимо наблюдение в динамике, то есть потребуется неоднократно с определенными промежутками сдавать кровь для исследования.
Принципы лечения заболевания
Сразу оговоримся, при этом диагнозе пациент нуждается в высококвалифицированной медицинской помощи и постоянном наблюдении. Поэтому не нужно полагаться на случай, считая, что опухоль рассосется и все пройдет. Самоустраниться очаг не может! При отсутствии адекватной терапии слишком велика опасность стать инвалидом с необратимыми функциональными нарушениями, летальные случаи от последствий тоже бывают.
В зависимости от степени тяжести клинической картины больным рекомендуется решение проблемы оперативным путем или/и консервативными методами. К базовым процедурам терапии относят:
- нейрохирургию – удаление аденомы трансназальным доступом (через нос) под эндоскопическим контролем или транскраниальным способом (делается стандартная трепанация черепа в лобной части) под контролем флюороскопа и микроскопа;
Трансназально оперируют 90% пациентов, 10% нуждаются в транскраниальной эктомии. Последняя тактика применяется при массивных опухолях (более 3 см), ассиметричном разрастании новообразованной ткани, выходе очага за пределы седла, опухолях с вторичными узлами.
- лечение медикаментами – использование лекарственных препаратов из ряда агонистов дофаминовых рецепторов, пептидсодержащих средств, целевых препаратов для коррекции гормонов;
- радиотерапию (лучевое лечение) – протонная терапия, дистанционная гамматерапия посредством системы Gamma Knife;
- комбинированное лечение – курс программы объединяет сразу несколько указанных терапевтических тактик.
Не использовать операцию, а рекомендовать наблюдение за человеком с диагнозом «аденома гипофиза», врач может при отсутствии очаговых неврологических и офтальмологических нарушений при гормонально-неактивном поведении опухоли. Ведение такого пациента осуществляет врач-нейрохирург в плотном сотрудничестве с эндокринологом и окулистом. Подопечного систематично обследуют (1-2 раз в год), направляя на МРТ/КТ, глазное и неврологическое обследование, измерение гормонов в крови. Параллельно с этим человек проходит курсами целенаправленную поддерживающую терапию.
Поскольку оперативное вмешательство является ведущим методом лечения аденомы гипофиза, вкратце осветим ход хирургического процесса эндоскопической операции.
Трансназальная операция по удалению аденомы гипофиза головного мозга
Это – миниинвазивная процедура, не требующая краниотомии и не оставляющая после себя никаких косметических дефектов. Выполняется чаще под местной анестезией, основным прибором хирурга будет эндоскоп. Нейрохирург через нос с помощью оптического устройства удаляет мозговую опухоль. Как же все это делается?
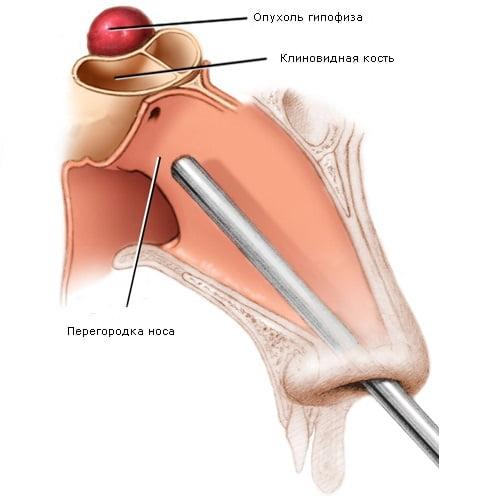
- Пациент в момент процедуры находится в положении сидя или полусидя. В полость носа аккуратно вводится тоненькая трубка эндоскопа (не более 4 мм в диаметре), снабженная на конце видеокамерой.
- Изображение очага и прилегающих структур в реальном времени будет передаваться на интраоперационный монитор. Хирург по мере продвижения эндоскопического зонда выполняет ряд последовательных манипуляций, чтобы подобраться к интересующей части мозга.
- Сначала отделяется слизистая оболочка носа с целью обнажения и вскрытия передней стенки. Затем тонкую костную перегородку перерезают. За ней находится искомый элемент – турецкое седло. В дне турецкого седла делается небольшое отверстие путем отделения маленького фрагмента косточки.
- Далее микрохирургическим инструментарием, помещенным в канал трубки эндоскопа, через образованный хирургом доступ постепенно отщепляются патологические ткани до полной ликвидации опухоли.
- На завершающем этапе созданное в днище седла отверстие перекрывается костным фрагментом, который фиксируют спецклеем. Носовые пути тщательно обрабатывают антисептиками, но не тампонируют.
Пациента активизируют в раннем периоде – уже на первые сутки после малотравматичной нейрооперации. Примерно на 3-4 сутки оформляется выписка из стационара, дальше понадобится пройти специальный курс реабилитации (антибиотикотерапию, физиотерапию и пр.). Несмотря на перенесенную хирургию по иссечению аденомы гипофиза, некоторым больным будет предложено дополнительно придерживаться гормонозаместительной терапии.
Риски интра- и послеоперационных осложнений при эндоскопической процедуре сведены до минимума – 1%-2%. Для сравнения, негативные реакции разного характера после транскраниальной резекции АГГМ возникают примерно у 6-10 чел. из 100 прооперированных пациентов.
После трансназального сеанса у большинства людей некоторое время наблюдается затруднение носового дыхания, неприятные ощущения в носоглотке. Причина – необходимое интраоперационное разрушение отдельных структур носа, как следствие, болезненные признаки. Дискомфорт в носоглоточной области обычно не расценивается как осложнение, если не усиливается и длится недолго (до 1-1,5 мес.).
Окончательно оценить эффект от операции возможно только через 6 месяцев по снимкам МРТ и результатам гормональных анализов. В целом, при своевременном и правильном проведении диагностики и оперативного вмешательства, качественной реабилитации, прогнозы благоприятные.
Заключение
Очень важно обратиться к лучшим специалистам по нейрохирургическому профилю. . Ехать за границу – мудрое решение, однако не каждый может осилить финансово, к примеру,лечение в Израиле или Германии.

Центральный Военный Госпиталь г.Прага.
Обратите внимание, не менее успешной в области нейрохирургии головного мозга является Чехия. В Чешской Республике благополучно оперируют аденомы гипофиза, используя самые передовые технологии аденомэктомии, причем так же технически безупречно и с минимумом рисков. Разница между Чехией и Германией/Израилем в том, что услуги чешских клиник как минимум вдвое обходятся дешевле, а медицинская программа всегда включает полноценную реабилитацию.